7月25日����,美國生物醫藥公司Checkpoint Therapeutics在其官網(wǎng)宣布�,公司核心項目PD-L1抗體藥物--Cosibelimab重新提交的BLA申請已被FDA受理��,適應癥為治療不適合進(jìn)行根治性手術(shù)或根治性放療的轉移性或局部晚期皮膚鱗狀細胞癌(cSCC)成人患者���,PDUFA日期為2024年12月28日���。
7月25日�,美國生物醫藥公司Checkpoint Therapeutics在其官網(wǎng)宣布�����,公司核心項目PD-L1抗體藥物--Cosibelimab 重新提交的BLA申請已被FDA受理���,適應癥為治療不適合進(jìn)行根治性手術(shù)或根治性放療的轉移性或局部晚期皮膚鱗狀細胞癌(cSCC)成人患者�����,PDUFA日期為2024年12月28日�。此前2023年12月�,FDA曾因第三方合同制造組織(CMO)制造問(wèn)題拒絕了Cosibelimab的BLA�����,但并未對Cosibelimab的臨床數據包���、安全性以及說(shuō)明書(shū)表示任何擔憂(yōu)��。
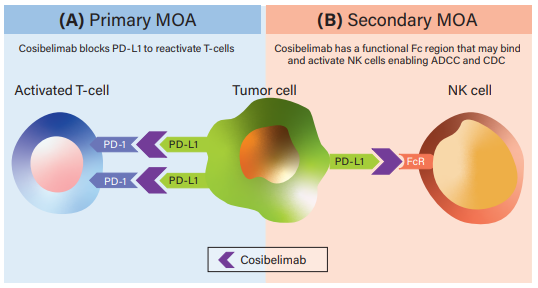
Cosibelimab是一款高親和力���、全人源化IgG1亞型單克隆抗體���,其作用機制主要體現在兩個(gè)方面:一是可直接結合PD-L1并阻斷PD-L1與PD-1和B7.1受體的相互作用����。從而消除PD-L1對抗腫瘤CD8+T細胞的抑制作用��,從而恢復細胞毒性T細胞反應��;二是Cosibelimab具有功能性Fc結構域����,可能能夠誘導針對腫瘤細胞的抗體依賴(lài)性細胞毒性(ADCC)和補體依賴(lài)性細胞毒性(CDC)���。
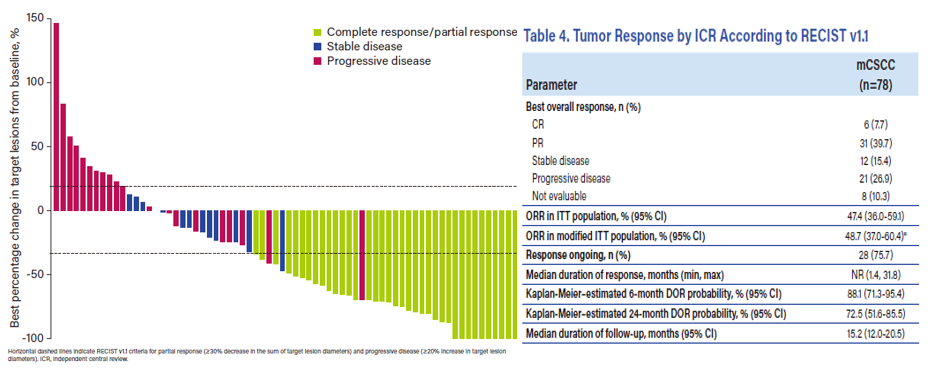
Cosibelimab治療皮膚鱗狀細胞癌的臨床數據早在2022年已報道����,研究共納入了78名mCSCC患者�����,確認客觀(guān)緩解率(ORR)為47.4%(95% CI:36.0���,59.1)����。2022年6月�����,臨床中期分析結果�����,根據對隊列中31名患者的獨立中央審查���,確認ORR為54.8%(95% CI:36.0�,72.7)��,超過(guò)了95%雙側置信區間25%的臨床意義下限�����。
參考文獻:
1. 2022年ASCO:Efficacy and Safety of Cosibelimab, an Anti–PD-L1 Antibody, in Patients With Metastatic Cutaneous Squamous Cell Carcinoma: Results From Pivotal Cohort
2.https://ir.checkpointtx.com/news-events/press-releases/detail/93/checkpoint-therapeutics-submits-biologics-license
如果這篇文章侵犯了您的權利���,請聯(lián)系我們�����。




![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博華國際展覽有限公司版權所有(保留一切權利)
滬ICP備05034851號-57
2006-2025 上海博華國際展覽有限公司版權所有(保留一切權利)
滬ICP備05034851號-57